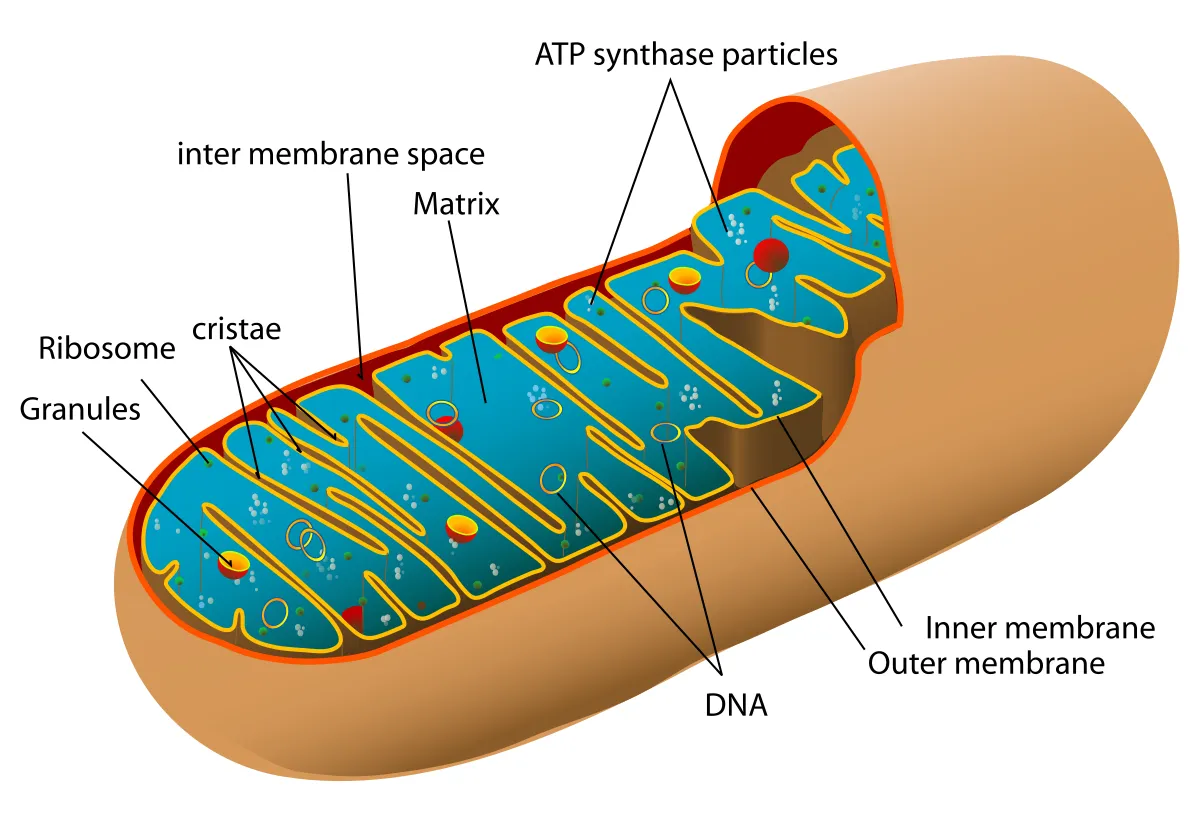
线粒体移动和损伤
线粒体在体内是如何移动的? 只在细胞内部移动吗? 可以去细胞外面吗?
线粒体在体内的移动机制复杂且多样化,不仅限于细胞内部,还能通过特定途径转移到其他细胞或细胞外环境。以下是其移动方式及范围的详细分析:
细胞内移动机制
线粒体在细胞内的运动依赖于细胞骨架系统:
- 微管网络:线粒体通过马达蛋白(如驱动蛋白KIF5B和动力蛋白Dynein)沿微管轨道运输,实现定向移动。
- 动态定位:根据细胞能量需求,线粒体可聚集在高耗能区域(如神经元突触)或分散至细胞边缘。
细胞间转移途径
线粒体可通过以下方式跨越细胞边界:
- 隧道纳米管(TNTs):细胞间形成的临时通道,直接运输线粒体和其他物质。
- 细胞外囊泡:线粒体被包裹在囊泡中释放,通过胞吐作用传递给邻近细胞。
- 自由漂浮:在血液等体液中,线粒体以游离形式存在并被其他细胞摄取。
细胞外释放与质量控制
- 迁移体介导的分泌:清华俞立团队发现,受损线粒体会被运输至迁移体(migrasome)并分泌到细胞外,这一过程称为“线粒体分泌”(mitocytosis),是线粒体质量控制的新机制。
- 选择性排出:受损线粒体因与KIF5B结合增强、与Dynein结合减弱,更易被运输至细胞边缘并进入迁移体。
生理与病理意义
- 组织修复:在中风模型中,星形胶质细胞通过隧道纳米管将线粒体转移给受损神经元,促进其恢复。
- 免疫调节:间充质干细胞的线粒体转移可抑制T细胞炎症反应,缓解类风湿性关节炎等疾病。
- 癌症进展:癌细胞可能通过获取健康细胞的线粒体增强代谢能力,促进转移。
人类研究的不确定性
尽管动物实验证实了线粒体转移的存在,但人体内直接观察仍受限。伦敦帝国理工学院研究者指出,目前技术难以实时追踪人体内的线粒体动态。
总结:线粒体不仅能在细胞内定向运输,还可通过隧道纳米管、囊泡或自由扩散跨越细胞边界,甚至进入血液循环。这种“多细胞器”特性为疾病治疗提供了新思路,但其在人类生理中的具体作用仍需进一步研究。

什么情况会导致 线粒体受损?
线粒体受损的原因多种多样,主要包括以下几类:
- 氧化应激与活性氧(ROS)过多线粒体是细胞内活性氧的主要产生场所,过量的ROS会损伤线粒体的DNA、蛋白质和膜脂,导致其结构和功能障碍。
- 钙离子失衡线粒体参与细胞内钙离子的调节,钙超载会引发线粒体通透性转变孔道(mPTP)开放,导致线粒体肿胀、膜电位丧失、能量生成障碍,最终引发细胞凋亡或死亡。
- 线粒体DNA突变或损伤线粒体DNA缺乏保护性组蛋白,修复能力较弱,容易受到ROS等因素的损伤。mtDNA突变累积会导致线粒体功能障碍。
- 线粒体嵴结构损伤线粒体嵴是其内膜的褶皱结构,嵴损伤会导致线粒体DNA释放到细胞质,激活炎症反应通路(如cGAS-STING),引发慢性炎症和衰老相关疾病。
- 缺血-再灌注损伤器官缺血后再恢复供血时,突增的氧气会产生大量ROS,造成线粒体氧化损伤和结构破坏。
- 外部毒素、药物或感染某些药物、环境毒素、病原体感染等可直接或间接损伤线粒体功能。
- 遗传因素与基因突变某些线粒体疾病由遗传性基因缺陷引起,影响线粒体的结构或功能。
- 衰老年龄增长会导致线粒体调节钙的能力下降,自由基生成增加,促进线粒体功能障碍。
- 炎症反应与免疫激活持续的线粒体受损会被免疫系统识别,诱发慢性炎症,进而损伤更多线粒体,形成恶性循环。
- 细胞凋亡机制异常激活线粒体在细胞凋亡中起核心作用,凋亡信号异常激活会导致线粒体膜通透性改变和功能丧失。
这些损伤因素常常相互作用,导致线粒体功能障碍,进而影响细胞和组织健康,甚至诱发多种疾病如神经退行性疾病、心血管疾病、代谢病等。
- Title: 线粒体移动和损伤
- Author: Salvio
- Created at : 2025-08-08 00:00:00
- Updated at : 2026-04-30 03:29:12
- Link: https://blog.ixsay.com/post/8489747d.html
- License: All Rights Reserved © Salvio
Comments